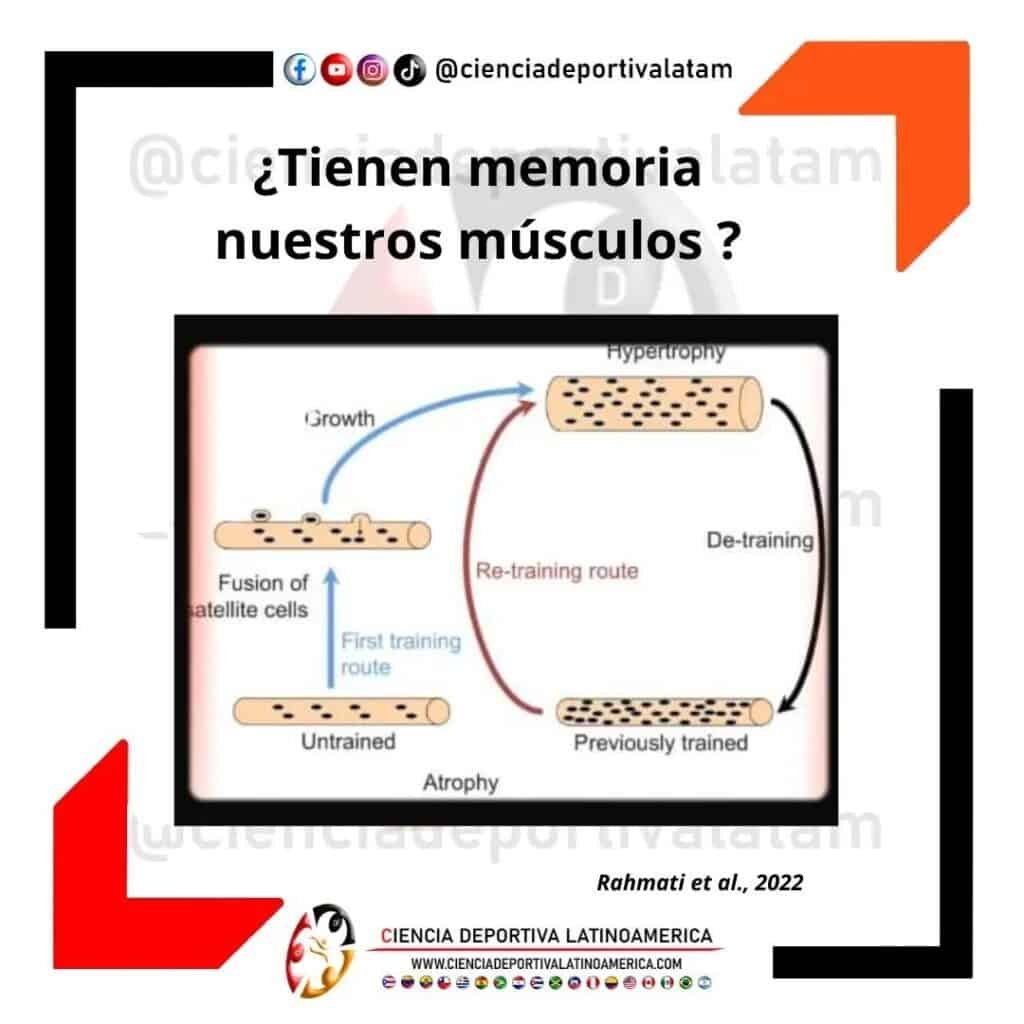
A la capacidad del tejido muscular esquelético para recuperar rápidamente las adaptaciones (particularmente de hipertrofia) alcanzadas tras un periodo de entrenamiento crónico, luego de un periodo de desentrenamiento, se le ha denominado «memoria muscular». Hace varios años se postularon dos mecanismos bastante plausibles que explicaban este fenómeno. La teoría de la adición mionuclear y la teoría epigenética, veamos brevemente de que se tratan:
ADICIÓN DE MIONÚCLEOS
Las fibras musculares son células multinucleadas. Es decir, poseen miles de núcleos para poder cubrir las demandas de síntesis proteica que requieren estas células supergigantes. Por tanto, cada núcleo se encarga de un segmento citoplasmático de la fibra muscular, lo que es denominado dominio mionuclear. Es como una gran empresa con muchos empleados, cada uno encargado de una oficina o sección específica de la empresa.
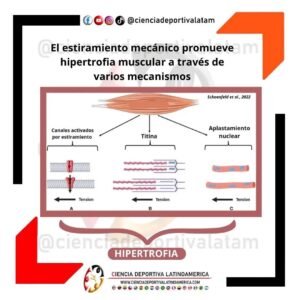
Cuando las fibras musculares son sometidas a estímulos mecánicos, como los inducidos por el entrenamiento de fuerza, estas sufren grandes daños estructurales, y en respuesta a esto, se activan células madre (células satélites), que proliferan para remodelar y reparar, y además se fusionan con fibras musculares dañadas, en aras de donar sus núcleos.
Así, las fibras musculares reparadas y de mayor tamaño, obtienen también una mayor cantidad de mionúcleos para cubrir la demanda proteica que supone su nuevo tamaño. La empresa ha crecido, y por tanto requiere de más empleados.
La teoría postula que, durante un periodo de desentrenamiento, estos mionúcleos nuevos obtenidos, no se pierden, ni sufren apoptosis durante la atrofia. A pesar de la pérdida de masa muscular, los mionúcleos parecen permanecer intactos (se ha reportado que hasta 15 años). Pese a que la empresa quiebra, los empleados no son despedidos. Una utopía si fuese más que un ejemplo.
Por eso es que, en un periodo de reentrenamiento, las fibras musculares pueden crecer más rápidamente que antes, pues tienen los suficientes mionúcleos, para suplir las demandas transcripcionales de una tasa de síntesis proteica aumentada por el estímulo de entrenamiento. Además, la información genética contenida en estos mionúcelos puede que este regulada epigenéticamente. Que es precisamente la segunda teoría que intenta explicar la «memoria muscular».
MEMORIA EPIGENÉTICA
Esta teoría es un tanto más compleja, pues tiene que ver con fisiología molecular. En palabras breves, es lo siguiente.
Los genes son secciones de ADN específicos, que son transcritos (decodificados) para sintetizar cadenas de ARN, que luego son traducidas a proteínas en el citosol de nuestras células. Básicamente, así es como a partir de la información genética contenida en el núcleo de nuestras células, se fabrican las proteínas que cumplen prácticamente todas las funciones que nuestros tejidos requieren para vivir. Un proceso llamado expresión genética.
Los genes pueden ser regulados para que puedan o no ser expresados. Una de estas formas de regulación, es el ambiente externo. Por lo cual, el ambiente puede modificar la expresión de nuestros genes y en consecuencia las proteínas fabricadas y, por tanto, las funciones de nuestros tejidos y órganos.
La suficiente exposición a un ambiente externo, como lo es el entrenamiento de fuerza programado y progresivo, influye en la regulación de la expresión genética.
Recientemente se han encontrado 5 genes específicos (que influyen en varios procesos anabólicos y están relacionados con la hipertrofia de fibras musculares), que permanecen regulados al alza, aun cuando se suspende el estímulo de entrenamiento. En otras palabras, imaginemos que nuestros genes tuviesen un interruptor de apagado y encendido. Pues bien, durante el desentrenamiento, estos 5 genes se mantienen con el interruptor encendido, por lo que luego cuando nos reentrenamos, están listos para ser expresados y responder a los estímulos de entrenamiento, y así promover la ganancia de masa muscular mucho más rápido. Esto se logra a partir de la modificación de proteínas ubicadas en la cromatina (cubierta de proteína de nuestro ADN), tales como las histonas. La modificación de histonas por parte del entrenamiento de fuerza, puede hacer que ciertos genes puedan permanecer regulados al alza.
A pesar de alguna acumulación de evidencia anecdótica y en modelos animales sobre el fenómeno de la preservación mionuclear, un nuevo metaanálisis ha encontrado que la investigación sobre este tema es bastante contradictoria y poco sólida para apoyar esta teoría. En realidad, parecen que los mionúcleos acumulados durante el entrenamiento, se pierden conjuntamente con la disminución de la masa muscular en los periodos de desentrenamiento.
En suma, se ha demostrado que la «memoria muscular» existe, pero todavía estamos lejos de dilucidar sus mecanismos potenciales. Por el momento, los cambios epigenéticos (modificaciones de segmentos del ADN para permitir la regulación de la expresión de genes) inducidos por el entrenamiento, parecen mantenerse a pesar del cese del estímulo de carga. Se requiere investigación para confirmar este mecanismo y otros que pueden contribuir, ya que muy seguramente este fenómeno fisiológico tiene su génesis en muchas vertientes simultáneas.
REFERENCIAS
Rahmati, M., McCarthy, J. J., & Malakoutinia, F. (2022). Myonuclear permanence in skeletal muscle memory: a systematic review and meta-analysis of human and animal studies. Journal of cachexia, sarcopenia and muscle, 13(5), 2276–2297. https://doi.org/10.1002/jcsm.13043
Schwartz LM (2019) Skeletal Muscles Do Not Undergo Apoptosis During Either Atrophy or Programmed Cell Death-Revisiting the Myonuclear Domain Hypothesis.Front. Physiol. 9:1887.doi: 10.3389/fphys.2018.01887
Murach KA, Englund DA, Dupont-Versteegden EE, McCarthy JJ and Peterson CA (2018) Myonuclear Domain Flexibility Challenges Rigid Assumptions on Satellite Cell Contribution to Skeletal Muscle Fiber Hypertrophy. Front. Physiol. 9:635. doi: 10.3389/fphys.2018.00635
Snijders T, Aussieker T, Holwerda A, Parise G, van Loon L, Verdijk LB. (2020) The concept of skeletal muscle memory: evidence from animal and human studies [published online ahead of print, Mar 16]. Acta Physiol (Oxf). 2020;10.1111/apha.13465. doi:10.1111/apha.13465.
Gundersen K. (2016). Muscle memory and a new cellular model for muscle atrophy and hypertrophy. J Exp Biol; 219(Pt 2):235–242. doi:10.1242/jeb.124495.
Turner DC, Seaborne RA, Sharples AP. (2019). Análisis comparativo de transcriptomas y metilomas en el anabolismo del músculo esquelético humano, hipertrofia y memoria epigenética. Sci Rep; 9 (1): 4251. Publicado el 12 de marzo de 2019 doi: 10.1038 / s41598-019-40787-0